Dichroman draselný
| Dichroman draselný | |
|---|---|
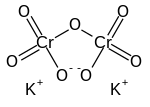 Strukturní vzorec | |
 Vzhled | |
| Obecné | |
| Systematický název | Dichroman draselný |
| Anglický název | Potassium dichromate |
| Německý název | Kaliumdichromat |
| Sumární vzorec | K2Cr2O7 |
| Vzhled | oranžovo-červená krystalická nebo práškovitá látka |
| Identifikace | |
| Registrační číslo CAS | 7778-50-9 |
| EC-no (EINECS/ELINCS/NLP) | 231-906-6 |
| PubChem | 516855 |
| UN kód | 3288 |
| Číslo RTECS | HX7680000 |
| Vlastnosti | |
| Molární hmotnost | 294,184 g/mol |
| Teplota tání | 398 °C |
| Teplota varu | > 600 °C (rozklad) |
| Teplota změny krystalové modifikace | 241,6 °C (α → β) |
| Hustota | 2,673 g/cm3 (α) 2,10 g/cm3 (β, 250 °C) |
| Index lomu | α-modifikace nDa= 1,720 2 (20 °C) nDb= 1,768 0 (20 °C) nDc= 1,819 7 (20 °C) β-modifikace nDa= 1,715 nDb= 1,762 nDc= 1,891 |
| Rozpustnost ve vodě | 4,58 g/100 g (0 °C) 12,22 g/100 g (20 °C) 35,61 g/100 g (50 °C) 46,46 g/100 g (60 °C) 70,90 g/100 g (80 °C) 95,59 g/100 g (100 °C) |
| Měrná magnetická susceptibilita | 1,357×10−6 cm3g−1 |
| Struktura | |
| Krystalová struktura | trojklonná (α) jednoklonná (β) |
| Hrana krystalové mřížky | α-modifikace a= 734 pm b= 749 pm c= 1 339 pm α= 96°20´ β= 97°56´ γ= 90°30´ β-modifikace a= 755 pm b= 749 pm c= 1 342 pm β= 91°42´ |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −2 061,5 kJ/mol |
| Standardní molární entropie S° | 289 JK−1mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −1 882 kJ/mol |
| Izobarické měrné teplo cp | 0,745 3 JK−1g−1 |
| Bezpečnost | |
 GHS03  GHS05  GHS06  GHS07  GHS08  GHS09 Nebezpečí[1] | |
| H-věty | H272 H350 H340 H360FD H330 H301 H372 H312 H314 H334 H317 H410 |
| R-věty | R45, R46, R60, R61, R8, R26, R25, R21, R34, R42/43, R48/23, R50/53 |
| S-věty | S53, S45, S60, S61 |
| NFPA 704 |  0 4 1 OX |
Některá data mohou pocházet z datové položky. | |
Dichroman draselný K2Cr2O7 je toxická, oranžovočervená krystalická látka, která se používá v analytické chemii jako primární oxidimetrický standard pro titrace, protože jej lze připravit ve velmi vysoké čistotě a je prakticky neomezeně stálý. Dichroman draselný se často používá jako oxidační činidlo v reakcích. Roztok dichromanu draselného ve zředěné kyselině sírové se používá rovněž jako testovací kyselina na stříbro, protože při reakci se stříbrem vzniká červená sraženina.
Bezpečnost
Dichroman draselný je jednou z nejčastějších příčin chromové dermatitidy;[2] chrom s vysokou četností vyvolává senzibilizaci vedoucí k dermatitidě, zejména na rukách a předloktích. Tato dermatitida je chronická a obtížně se léčí. Dichroman draselný je též toxický (zejména při vdechování), pro hlodavce je průměrná smrtelná dávka 100 mg/kg.[3]
Podobně jako jiné sloučeniny s šestimocným chromem, je dichroman draselný karcinogenní a mělo by se s ním pracovat jen s použitím náležitých ochranných prostředků. Je také žíravý a při zasažení oka může způsobit těžké poškození nebo i slepotu.[4]
Reference
V tomto článku byl použit překlad textu z článku Potassium dichromate na anglické Wikipedii.
- ↑ a b Potassium dichromate. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ Farokh J. Master. Diseases of Skin. New Delhi: B Jain Pub Pvt Ltd, 2003. Dostupné online. ISBN 8170211360. S. 223.
- ↑ Safety data for potassium dichromate Archivováno 23. 4. 2012 na Wayback Machine. HSci project
- ↑ Potassium dichromate MSDS [online]. JT Baker [cit. 2010-12-07]. Dostupné v archivu pořízeném dne 2010-11-23.
Literatura
- VOHLÍDAL, Jiří; ŠTULÍK, Karel; JULÁK, Alois. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
Externí odkazy
 Obrázky, zvuky či videa k tématu dichroman draselný na Wikimedia Commons
Obrázky, zvuky či videa k tématu dichroman draselný na Wikimedia Commons
 | Tento článek je příliš stručný nebo postrádá důležité informace. Pomozte Wikipedii tím, že jej vhodně rozšíříte. Nevkládejte však bez oprávnění cizí texty. |
| Anorganické soli draselné | |
|---|---|
| Halogenidy a pseudohalogenidy | Hydrogendifluorid draselný (KHF2) • Fluorid draselný (KF) • Bromid draselný (KBr) • Chlorid draselný (KCl) • Jodid draselný (KI) • Kyanid draselný (KCN) • Kyanatan draselný (KOCN) • Isokyanát draselný (KNCO) • Fulminát draselný (KCNO) • Thiokyanatan draselný (KSCN) • Isothiokyanatan draselný (KNCS) |
| Soli kyslíkatých kyselin (neuvedeny soli | Chlornan draselný (KOCl) • Chloritan draselný (KClO2) • Chlorečnan draselný (KClO3) • Chloristan draselný (KClO4) • Bromnan draselný (KOBr) • Bromitan draselný (KBrO2) • Bromičnan draselný (KBrO3) • Jodičnan draselný (KIO3) • Hydrogendijodičnan draselný (KHI2O6) Jodistan draselný (KIO4) • Siřičitan draselný (K2SO3) • Hydrogensiřičitan draselný (KHSO3) • Disiřičitan draselný (K2S2O5) • Dithioničitan draselný (K2S2O4) • Dithionan draselný (K2S2O6) • Síran draselno-hlinitý (KAl(SO4)2) • Síran draselný (K2SO4) • Hydrogensíran draselný (KHSO4) • Disíran draselný (K2S2O7) • Peroxosíran draselný (K2SO5) • Hydrogenperoxosíran draselný (KHSO5) • Peroxodisíran draselný (K2S2O8) • Seleničitan draselný (K2SeO3) • Selenan draselný (K2SeO4) • Telluričitan draselný (K2TeO3) • Metatelluran draselný (K2TeO4) • Tetrahydrogenorthotelluran draselný (K2H4TeO6) • Dusitan draselný (KNO2) • Dusičnan draselný (KNO3) • Orthodusičnan draselný (K3NO4) • Peroxydusitan draselný (KOONO) • Fosfornan draselný (KPO2H2) • Dihydrogenfosforitan draselný (K2PO3) • Hydrogenfosforitan draselný (K2HPO3) • Dihydrogenfosforečnan draselný (KH2PO4) • Hydrogenfosforečnan draselný (K2HPO4) • Fosforečnan draselný (K3PO4) • Dihydrogendifosforečnan didraselný (K2H2P2O7) • Hydrogendifosforečnan tridraselný (K3HP2O7) • Difosforečnan draselný (K4P2O7) • Trifosforečnan draselný (K5P3O10) • Metafosforečnan draselný (KPO3) • Cyklotrifosforečnan draselný (K3P3O9) • Cyklohexafosforečnan draselný (K6P6O18) • Arsenitan draselný (KAsO2) • Dihydrogenarseničnan draselný (KH2AsO4) • Hydrogenarseničnan draselný (K2HAsO4) • Arseničnan draselný (K3AsO4) • Hexahydrogenantimoničnan draselný (KSb (OH)6) • Antimonitan draselný (KSbO2) • Bismutičnan draselný (KBiO3) • Uhličitan draselný (K2CO3) • Hydrogenuhličitan draselný (KHCO3) • Šťavelan draselný (K2(CO2)2) • Hydrogenšťavelan draselný (KH(CO2)2) • Orthokřemičitan draselný (K4SiO4) • Metakřemičitan draselný (~K2SiO3~) • Dikřemičitan draselný (K2Si2O5) • Trikřemičitan draselný (K2Si3O7) • Cínatan draselný (K2SnO2) • Cíničitan draselný (K2SnO3) • Metaboritan draselný (KBO2) • Tetraboritan draselný (K2[B4O5(OH)4]•8H2O) • Oktaboritan draselný (K2B8O13•4H2O) • Perboritan draselný (K2H4B2O8) • Hlinitan draselný (K2Al2O4) • Tetrahydroxidozinečnatan draselný (K2Zn(OH)4) • Zinečnatan draselný (K2ZnO2) • Železičitan draselný (K2FeO3) • Železan draselný (K2FeO4) • Osman draselný (K2OsO4) • Manganitan draselný (~KMnO2~) • Manganečnan draselný (K3MnO4) • Manganan draselný (K2MnO4) • Manganistan draselný (KMnO4) • Technecistan draselný (KTcO4) • Rhenistan draselný (KReO4) • Chromitan draselný (K3[Cr(OH)6]) • Chroman draselný (K2CrO4) • Dichroman draselný (K2Cr2O7) • Molybdenan draselný (K2MoO4) • Wolframan draselný (K2WO4) • Metavanadičnan draselný (KVO3) • Orthovanadičnan draselný (K3VO4) • Trititaničitan draselný (K2Ti3O7) • Zirkoničitan draselný (K2ZrO3) • Berylnatan draselný (K2BeO2) |
| Soli tvořené záměnou vodíku ze sloučenin typu prvekx – vodíky | Hydrid draselný (KH) • Hydroxid draselný (KOH) • Oxid draselný (K2O) • Peroxid draselný (K2O2) • Superoxid draselný (KO2) • Ozonid draselný (KO3) • Hydrogensulfid draselný (KSH) • Sulfid draselný (K2S) • Selenid draselný (K2Se) • Tellurid draselný (K2Te) • Polonid draselný (K2Po) • Amid draselný (KNH2) • Imid draselný (K2NH) • Nitrid draselný (K3N) • Azid draselný (KN3) • Fosfid draselný (K3P) • Tetrahydridoboritan draselný (KBH4) • Tetrahydridohlinitan draselný (KAlH4) |









