フッ化コバルト(III)
| フッ化コバルト(III) | |
|---|---|
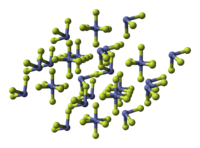 | |
別称 三フッ化コバルト | |
| 識別情報 | |
| CAS登録番号 | 10026-18-3 |
| 特性 | |
| 化学式 | CoF3 |
| モル質量 | 115.93 g/mol |
| 密度 | 3.88 g/cm3 |
| 融点 | 926 °C |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
フッ化コバルト(III)(フッかコバルト さん、cobalt(III) fluoride)は、化学式が CoF3 の無機化合物である。反応性の高い吸湿性の茶色の固体で、有機フッ素化合物の合成に使われる[1]。
合成
実験室では塩化コバルト(II) とフッ素を250°Cで反応させることによって合成する。
この過程は酸化還元反応であり、Co2+ が Co3+ へと酸化されるとともに Cl− も Cl2 へと酸化される。同様にフッ素を使うことにより、酸化コバルト(II) CoO や フッ化コバルト(II) からもフッ化コバルト(III) を合成できる。
反応
フッ素化剤
CoF3 は強力なフッ素化剤であり、反応後にフッ化コバルト(II) CoF2 を生成する。水と接触すると分解し、酸素を放出する。
吸湿
CoF3 は吸湿性であり、錯イオン [CoF6]3− に変換することもできる。これは高スピン型八面体コバルト(III) 錯体の稀な例である。
スラリー状の CoF3 は、炭化水素のペルフルオロカーボンへの変換に使われる。
この反応ではしばしば転位反応など他の化学反応と同時に起こる[1]。関連した試薬にKCoF4があり、こちらの方がより選択性が高い[2]。
出典
- ^ a b Coe, P. L. (2004). "Cobalt(III) Fluoride." In Encyclopedia of Reagents for Organic Synthesis. Paquette, L. ed. J. Wiley & Sons: New York. doi:10.1002/047084289.
- ^ Coe, P. L. (2004). "Potassium Tetrafluorocobaltate(III)." In Encyclopedia of Reagents for Organic Synthesis. Paquette, L. ed. J. Wiley & Sons: New York. doi:10.1002/047084289.
関連項目
- フッ化コバルト(II)
- ファウラー法
外部リンク
- National Pollutant Inventory - Cobalt fact sheet
- National Pollutant Inventory - Fluoride and compounds fact sheet












